カシス
英名
Black currant
学名
Ribes nigrum L.
科目
スグリ科
別名
クロスグリ、クロフサスグリ
原産地
ポーランド、ニュージーランド、カナダ、日本(青森県)
利用部位
葉、果実
成分
■アントシアニン (果実) 2)
delphinidin-3-O-glucoside
delphinidin-3-O-rutinoside
cyanidin-3-O-glucoside
cyanidin-3-O-rutinosid
■プロデルフィニジン(葉) 3)
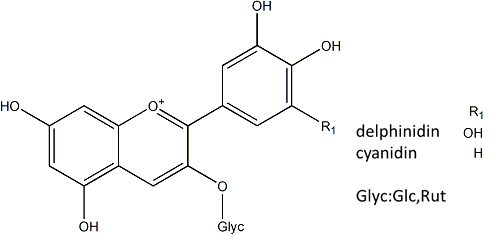
図1 カシス含有成分
花言葉
『あなたの不機嫌が私を苦しめる』『あなたは私を喜ばせる』『あなたに嫌われたら生きていけない』
見ごろ
5月(開花)、7~8月(収穫)
カシスは高さ1.5~2.0 mの落葉低木で、7・8月には直径1.0 cmほどの赤黒く酸味の強い果実を実らせる。果実に対して大きな種には、オレイン酸、リノール酸などの栄養素が多く含まれる。花は緑白色で総状花序をなし、果肉はうすく緑色づき果皮にはアントシアニンが豊富に含まれる。ヨーロッパ、西アジア、中央アジア、ヒマラヤなどに自生しており、また多くの温暖な地域で栽培されている。

~伝統的な健康果実~
カシスはブルーベリーやラズベリーなどと一緒にベリー系と総称されることがあるが、カシスはスグリ科、ブルーベリーはツツジ科、ラズベリーはバラ科とそれぞれ別の科に属する。収穫時期が短く、さらに甘みが少なく酸味が強いカシスは、ブルーベリーのように生で食べる事はあまりなく、ジャムやリキュール、スイートソースなど加工されて使われることが多い。また、カシスは、16世紀後半から17世紀にかけて活躍したスイスの植物学者ガスパール・ポアンによって広められ、薬草として病気の予防効果を期待され積極的に用いられた。特にリキュールは保存可能なため、必要な時に使用できる貴重な民間薬としての役割をもっており、修道士の活動を通じて身体の健康の維持に役立つものとして広く認識された。果実はビタミンCやビタミンA、ビタミンB1を豊富に含む他、ミネラル類も他のベリーと比べて多く含む。さらに近年抗酸化物質として注目されているアントシアニンが多く含まれる。空気が澄み紫外線量の多いニュージーランドで育ったカシスは、夏の強い紫外線から果実を守るためにアントシアニンが蓄えられ、他の産地で育つカシスよりも高いアントシアニン含有量を誇る。
流通品規格
アントシアニンの規定が設けられる。
以下の項目は、その植物の期待される効果を示すものです。
作用
- ・脂肪燃焼作用14)
- ・運動能力向上作用15)
- ・酸化ストレス抑制作用16)
- ・筋肉疲労軽減作用17)
- ・血管拡張作用18)
- ・精神的疲労感改善19)
● 葉
- ・止瀉作用
- ・抗炎症作用
● 果実
- ・眼精疲労改善作用
- ・視覚機能改善作用
- ・血流改善作用
- ・抗ウィルス作用
- ・止瀉作用
生理活性機能
● 視覚サイクルの改善(果実)
cyanidin rutinosideは他の植物では含まれていることが少ないブラックカーラント特有のアントシアニンである。in vitroの試験において、このcyanidin rutinosideには眼球内網膜に存在する視覚物質の一つロドプシンの再合成を促進させる機能があることが認められており(図2)4)、暗順応の改善、夜間視力の改善等の効果が期待できる。
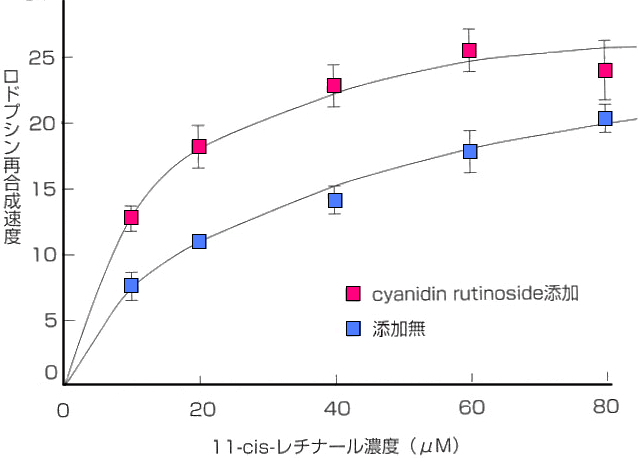
図2 cyanidin rutinoside添加によるロドプシン再合成速度の変化
それぞれの11-cis-レチナール濃度において、cyanidin rutinosideの添加はコントロールと比較して ロドプシン再合成速度を速めている。
● 抗ウィルス活性(果実)
in vitroの試験において、ブラックカーラント果汁には抗インフルエンザウィルス活性、抗単純ヘルペスウィルス活性があることが報告されている。この活性は細胞内に進入したウィルスの増殖を抑制することが示唆されている 5) 6)。
● 抗ウィルス活性(葉)
in vitro、in vivoの試験において、抗インフルエンザ活性(A型)があることが報告されている。ブラックカーラント葉抽出物を添加した細胞においてインフルエンザ感染初期の抵抗性を増大することが示唆されている 7)。
● 血流改善作用(果実)
高脂肪食を与えたサルの試験において、高脂肪食のみを与えたサルの血液の濾過性が悪化したのに対し、高脂肪食とブラックカーラント果実抽出物を与えたサルは濾過性の悪化が抑制されたことが報告されている8)。
● 抗炎症作用(葉)
前脚にカラゲニンを注入された炎症モデルラットを用いた試験において、注入前にブラックカーラント葉抽出物を経口投与したラットは、コントロール群と比べて浮腫の誘発が抑制されることが確認されている9)。
また、ブラックカーラントの葉に含まれるプロデルフィニジン類は、ヒト軟骨細胞を用いた試験において、骨関節症に有効であることを示唆している10)。
臨床試験
○ 視覚機能改善作用(果実)11) 12)
健常な12人の被験者にブラックカーラント果実抽出物を摂取させ、摂取2時間後の暗所閾値の測定を行 った。この結果、アントシアニン50mg投与群で、偽薬群と比較して有意に暗順応が改善されていることが認められた(表1)。
表1 ブラックカーラント果実抽出物の暗順応改善効果
| 摂取量 | 暗所闘値 log asb (apostilb)、平均± SD ; (p値) | |||
mg/人 | 摂取前 | 摂取後 | 変化量 | p値 |
偽薬 | 2.056±0.209 | 2.018±0.218 | -0.038±0.106 | 0.244 |
12.5 | 2.026±0.170 | 2.004±0.195 | -0.023±0.138 | 0.538 |
25 | 2.016±0.170 | 1.980±0.197 | -0.037±0.012 | 0.280 |
50 | 2.038±0.186 | 1.923±0.167 | -0.037±0.112 | 0.011 |
※1 括弧内は縦の各カラムで偽薬群を標準として統計的p値を示す
※2 同一摂取量の摂取前と摂取後で比較したときの統計的p値を示す
また健常な21人を被験者に2時間のパソコン作業(視覚負荷作業)を行わせたところ、ブラックカーラント果実抽出物投与群は偽薬群に比べ、レンズ屈折値の低下が抑制されており、パソコン作業による一時的な仮性近視が緩和されているのが認められた。また、パソコン作業による眼精疲労に関する自覚症状も有意に改善されているのが認められた。
○ 脂肪燃焼作用14)
運動習慣のある男性15名を対象とした、脂質酸化に関する無作為化カウンターバランス試験が行われた。被験者はニュージーランド産カシスエキス0mg/日、300 mg/日、600 mg/日、900 mg/日をそれぞれ7日間摂取した。各摂取期間の後サイクリングを120分間実施し15分間隔で二酸化炭素排出量、最大酸素摂取量を測定し、脂質酸化量を算出した。その結果、ニュージーランド産カシスエキス摂取による、有意な脂質酸化量の増加がみられ(P < 0.05)、運動による脂肪代謝を高める可能性が示唆された。
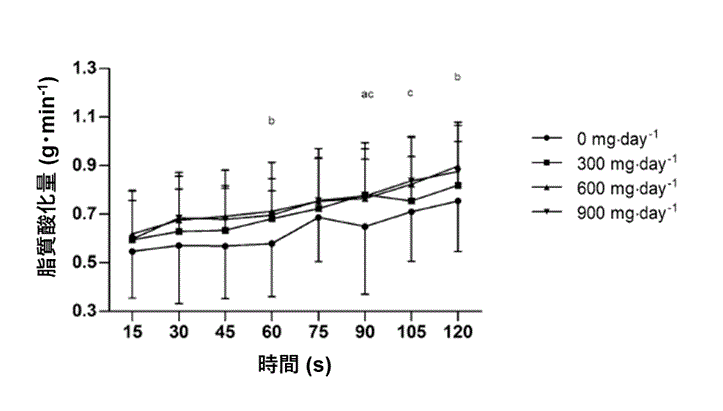
図3 ニュージーランド産カシスエキス投与による脂質酸化量の増加
a,b,c: P<0.05(それぞれ0 mg/日と300 mg/日、300 mg/日と600 mg/日、600 mg/日と900 mg/日の比較)
○ 運動能力向上作用15)
健常な成人男性14名を対象として運動能力を検証する無作為化二重盲検プラセボ対照交差試験が行われた。被験者は7日間ニュージーランド産カシスエキス300 mgまたはプラセボを含んだカプセルを朝食時に1粒摂取した。、摂取7日目に30分間のサイクリングを行い、15分間の休憩の後、16.1 kmサイクリング走の走破時間を測定した。この結果、ニュージーランド産カシスエキスの摂取により、16.1 kmサイクリング走の走破時間が有意に短くなり(P < 0.05)、運動能力の向上が示された。
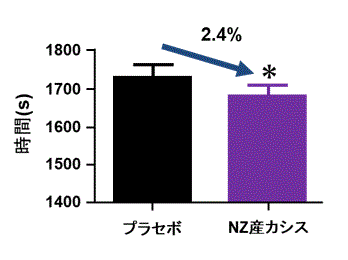
図4 ニュージーランド産カシスエキス投与による16.1 kmサイクリング走破時間の短縮
*P<0.05 プラセボとの比較
○ 酸化ストレス軽減作用16)
健常な成人男女10名を対象として運動時の酸化ストレスについての二重盲検交差試験が行われた。被験者はニュージーランド産カシスエキス(アントシアニンを60 mg含む)またはプラセボを運動前及び運動後に2粒摂取した。運動開始前及び運動終了直後、運動開始後1,2,24時間後における血液採取を行い、運動による酸化ストレスを反映する血中カルボニル化タンパク質濃度及び血液中の活性酸素種(ROS)生成能を測定した。その結果、血中タンパク質カルボニル濃度及びROS生成能はニュージーランド産カシスエキスの摂取によって有意に低下し(P < 0.05)、酸化ストレスの軽減が示された。
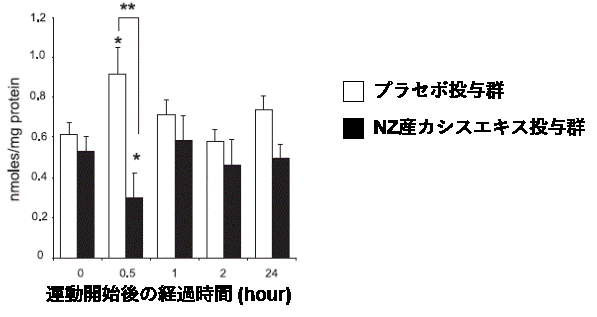
図5 ニュージーランド産カシスエキス投与による血中タンパク質カルボニル濃度の減少
*P<0.05 運動前後の比較
**P<0.05 プラセボとの比較
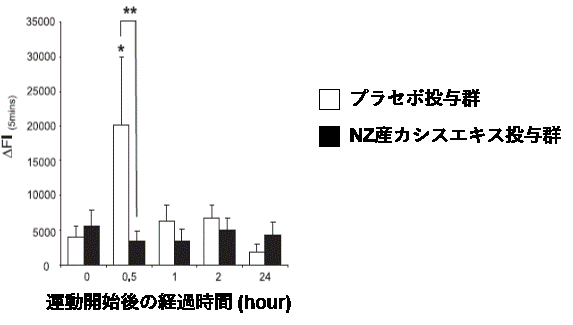
図6 ニュージーランド産カシスエキス投与によるROS生成能の減少
*P<0.05 運動前後の比較
**P<0.05 プラセボとの比較
○ 筋肉疲労軽減作用17)
健常な成人10名に、5日間ニュージーランド産カシスエキス(アントシアニンを240 mg含む)を摂取した後、運動による筋肉損傷を調べた。摂取前後及び運動後に血液採取を行い血液中のクレアチンキナーゼ濃度及び、ミオグロビン濃度を測定することにより筋肉損傷を評価した。。この結果、筋肉損傷が起きると血中に分泌されるクレアチンキナーゼ及びミオグロビンの濃度は減少した。以上より、ニュージーランド産カシスエキスの摂取による筋肉疲労軽減作用が示された。
○ 血管拡張作用18)
健常な成人男性13名を対象とした無作為化二重盲検プラセボ対照交差試験が行われた。7日間ニュージーランド産カシスエキス300 mgを含むカプセル(ニュージーランド産カシスエキス由来アントシアニン 105 mg含む)を2粒/日摂取し、7日後に120秒間の持続性等尺性収縮負荷中の心血管反応を評価した。ニュージーランド産カシスエキス摂取群は大腿動脈の直径及び心拍出量の増加さらに血圧を低下させ、ニュージーランド産カシスエキスによる血管拡張作用が示唆された。
○ 精神的疲労感改善19)
健常な成人男女36名を対象として無作為化二重盲検プラセボ対照交差試験を実施し、精神的な疲労感を評価した。、3日間ニュージーランド産カシスエキス 1.66 g/日 (アントシアニン 571 mg含む)を摂取し、摂取前後に精神的な疲労度をVASによって評価した。その結果、プラセボ摂取群と比較しニュージーランド産カシスエキス摂取群はVAS値が有意に減少し(P<0.05)、ニュージーランド産カシスエキスの摂取による精神的疲労感の軽減作用が示された。
安全性
果汁、花、葉がGRAS (FDAが定めた一般的に安全とみなされた物質) として認定されており、通常の食品として適切に摂取すれば安全であるとされる20)。
ラットを用いた毒性試験の結果、最小中毒量(TDL0)は10 mg/kg 20)であった。
引用文献・ 参考文献
1)Traitler H.Lipids, 19, 923 (1984)
2)Slimestad R. et al.,J. Agric. Food. Chem., 50, 3228 (2002)
3)Tits M. et al.,Journal of Pharmaceutical &Biomedical Analysis.,10, 1097 (1992)
4)Matsumoto H. et al.,J. Agric. Food. Chem.,51, 3560 (2003)
5)Knox Y. M. et al.,Phytother. Res., 17, 120 (2003)
6)Knox Y. M. et al.,Phytother. Res., 17, 609 (2003)
7)Christina E.et al.,PLOS ONE, 8 , 5 , e63657 (2013)
8)Millet J. et al.,J. Pharmacol.,14, 439 (1984)
9)Declume C. et al.,Journal Ethno pharmacology,27, 91 (1989)
10)Garbacki N. et al.,Naunyn-Schmiedeberg’s Arch Pharmacol,365, 434 (2002)
11)Nakanishi H. et al.,Alter. Med. Rev,5553(2000)
12)平山匡夫ら,食品工業 ,44, 56 (2001)
13)Dr Roger H.et al.,Foodstyle21,15, 3 (2011)
14) David M. et al., European Journal of Applied Physiology, 117(6), 1207-1216 (2017)
15) Matthew D.C et al., European Journal of Applied Physiology, 115(11), 2357-2365 (2015)
16) Lyall K.A. et al., American Journal of Physiology-Regulatory, Integrative and Compare Physiology, 297(1), 70-81 (2009)
17) Hurst S. M. et al., Anthocyanins in health and disease, TC Wallace (Ed.) CRC Press (2013)
18) Matthew D.C. et al., Nutrients, 9(6), 556-569 (2017)
19)Watson A.W. et al., Journal of Functional Foods, 17, 524-539 (2015)
20) 国立研究開発法人 医薬基盤・健康・栄養研究所「健康食品」の安全性・有効性情報
